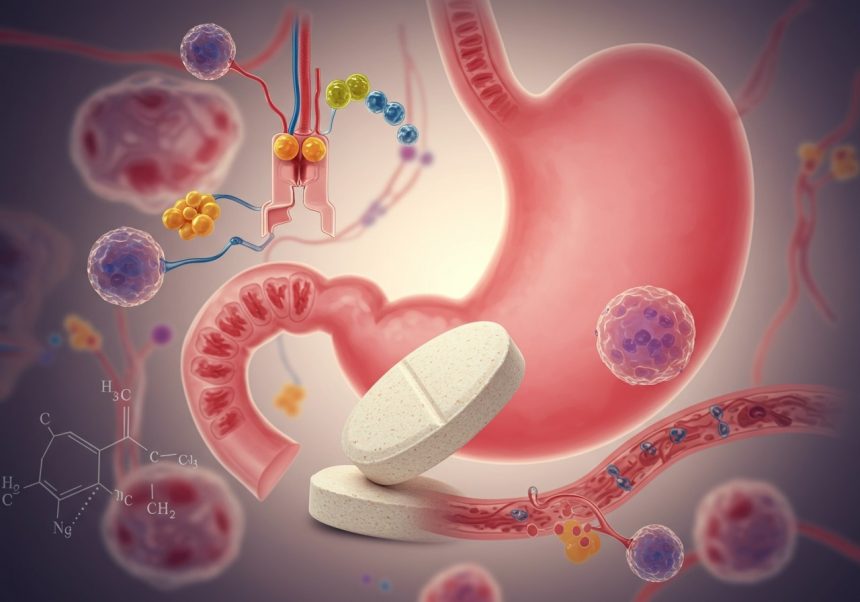
A gyomorsav, más néven sósav (HCl), kulcsfontosságú szerepet játszik az emésztésben. Egyrészt segít a fehérjék denaturálásában, ami előkészíti őket az enzimek általi lebontásra. Másrészt elpusztítja a gyomorba kerülő káros baktériumokat és egyéb kórokozókat, így védelmet nyújt a fertőzésekkel szemben. A gyomorsav ezen felül aktiválja a pepszinogént pepszinné, ami egy fehérjebontó enzim.
Bár a gyomorsav elengedhetetlen, a túlzott savtermelés komoly problémákat okozhat. A gyomornyálkahártya védelmet nyújt a sav maró hatása ellen, de ha ez a védelem sérül, vagy ha a savtermelés túlzott, gyomorfekély, gyomorégés, reflux és egyéb kellemetlen tünetek jelentkezhetnek. Ezért a gyomorsav szintjének szigorú szabályozása létfontosságú az egészség megőrzése szempontjából.
A szervezetnek finomhangolt mechanizmusokkal kell biztosítania, hogy a gyomorsav termelése elegendő legyen az emésztéshez és a védelemhez, de ne károsítsa a gyomor falát.
A gyomorsav szintjének szabályozása egy összetett folyamat, amelyben több tényező is szerepet játszik. Ide tartoznak hormonális hatások (pl. gasztrin), idegi impulzusok (pl. vagus ideg) és maga a gyomor pH-értéke is. Ezek a tényezők mind befolyásolják a parietális sejtek működését, amelyek a gyomorsavat termelik. A parietális sejtekben található protonpumpa (H+/K+-ATPáz) pedig a gyomorsav termelésének központi eleme, és célzott szabályozásának köszönhetően a savszint hatékonyan kontrollálható.
A gyomor anatómiája és a parietális sejtek felépítése
A gyomor egy komplex szerv, melynek belső felszínét nyálkahártya borítja. Ez a nyálkahártya számos apró gödröcskét tartalmaz, melyek a gyomormirigyekbe vezetnek. Ezek a mirigyek felelősek a gyomornedv termeléséért, ami elengedhetetlen a táplálék emésztéséhez. Több fajta sejt található a gyomormirigyekben, de a parietális sejtek (más néven fedősejtek) kulcsszerepet játszanak a gyomorsav (sósav, HCl) termelésében. Ezek a sejtek a gyomormirigyek középső részén helyezkednek el.
A parietális sejtek felépítése rendkívül specializált. Jellemzőjük a kiterjedt intracelluláris csatornahálózat, a canaliculi, melyek jelentősen megnövelik a sejt felszínét. Ezenkívül rengeteg mitokondriummal rendelkeznek, ami az intenzív energiaigényes savtermeléshez szükséges. A canaliculi membránjában található a H+/K+-ATPáz enzim, közismertebb nevén a protonpumpa. Ez a pumpa aktív transzporttal juttatja a hidrogénionokat (H+) a gyomor lumenébe, miközben káliumionokat (K+) szállít vissza a sejtbe. A kloridionok (Cl–) passzívan követik a hidrogénionokat, így alakul ki a gyomorsav (HCl).
A parietális sejtek működését különböző hormonok és neurotranszmitterek szabályozzák. A gasztrin, a hisztamin és az acetilkolin stimulálják a savtermelést, míg a szomatosztatin gátolja azt. Ezek a szabályozó anyagok a parietális sejtek felszínén található receptorokhoz kötődve fejtik ki hatásukat, beindítva vagy leállítva a protonpumpa működését.
A parietális sejtek rendkívül specializált sejtjei a gyomornedvtermelő mirigyeknek, melyek a protonpumpa segítségével aktívan termelik és juttatják a sósavat (HCl) a gyomor lumenébe.
A protonpumpa tehát nem csupán egy enzim, hanem a gyomorsavtermelés központi eleme. A gyógyszeripar által kifejlesztett protonpumpa-gátlók (PPI-k) közvetlenül ezt az enzimet célozzák meg, csökkentve a gyomor savszintjét. Ezáltal hatékonyan kezelhetők a savtúltermeléssel járó betegségek, mint például a gyomorfekély vagy a reflux.
A protonpumpa (H+/K+ ATPáz) részletes bemutatása: szerkezet és működési mechanizmus
A gyomorsav termelésének központi eleme a protonpumpa, más néven H+/K+ ATPáz. Ez egy membránfehérje, amely a gyomor parietális sejtjeinek apikális membránjában található, és felelős a hidrogénionok (H+) aktív transzportjáért a gyomor lumenébe, a gyomorsav szekréciójának végső lépéséért.
A protonpumpa egy heterodimér fehérje, amely egy alfa (α) és egy béta (β) alegységből áll. Az α alegység katalitikus alegységként működik, tartalmazza az ATP kötőhelyét és a H+/K+ ionok transzportjához szükséges aminosavakat. A β alegység fontos szerepet játszik a fehérje megfelelő konformációjának kialakításában, a sejtmembránba történő beépülésében és a savas környezettel szembeni stabilitás biztosításában.
A működési mechanizmus során a protonpumpa az ATP hidrolízis energiáját használja fel a H+ ionoknak a parietális sejt citoplazmájából a gyomor lumenébe történő szállítására, miközben K+ ionokat szállít a lumenből a citoplazmába. Ez egy elektrogén folyamat, mivel nettó töltésmozgás történik a membránon keresztül.
A protonpumpa működése ciklikus, több lépésből áll:
- E1 konformáció: Ebben az állapotban a pumpa a citoplazma felé nyitott, és nagy affinitással rendelkezik a H+ ionokhoz.
- H+ kötés és ATP kötés: A H+ ionok megkötődnek, majd az ATP is kötődik a pumpához.
- Foszforiláció: Az ATP hidrolizálódik, és a felszabaduló foszfátcsoport a pumpa egy specifikus aminosavához kapcsolódik (foszforiláció).
- E2 konformáció: A foszforiláció konformációs változást idéz elő, amely a pumpát a gyomor lumenje felé nyitja. A H+ ionok a lumenbe kerülnek.
- K+ kötés: A pumpa lumen felé néző része K+ ionokat köt meg.
- Defoszforiláció: A foszfátcsoport leválik, ami újabb konformációs változást eredményez.
- K+ felszabadulás és E1 konformáció: A K+ ionok a citoplazmába kerülnek, és a pumpa visszatér az E1 konformációba, készen a következő ciklusra.
A gyomorsavszekréciót számos tényező szabályozza, beleértve a hormonokat (gasztrin, hisztamin), a neurotranszmittereket (acetilkolin) és a helyi mediátorokat. Ezek a tényezők a parietális sejtekben lévő receptorokhoz kötődve jelátviteli útvonalakat aktiválnak, amelyek végső soron a protonpumpa aktivitását befolyásolják. A gyógyszerek, például a protonpumpa-gátlók (PPI-k), közvetlenül a protonpumpához kötődnek, és irreverzibilisen gátolják annak működését, ezáltal csökkentve a gyomorsavtermelést.
A protonpumpa aktivitásának gátlása a gyomorsavszekréció hatékony csökkentésének kulcsfontosságú módja, amelyet széles körben alkalmaznak a gyomorfekély, a reflux betegség és más savval kapcsolatos betegségek kezelésében.
Fontos megjegyezni, hogy a protonpumpa nem csak a H+ ionok szállításáért felelős, hanem a gyomor pH-jának homeosztatikus szabályozásában is kulcsfontosságú szerepet játszik. Az általa létrehozott savas környezet elengedhetetlen a pepsinogén pepsinévé történő aktiválásához, amely az egyik fő fehérjebontó enzim a gyomorban.
A gyomorsav szekréciójának főbb stimuláló tényezői: hisztamin, acetilkolin, gasztrin
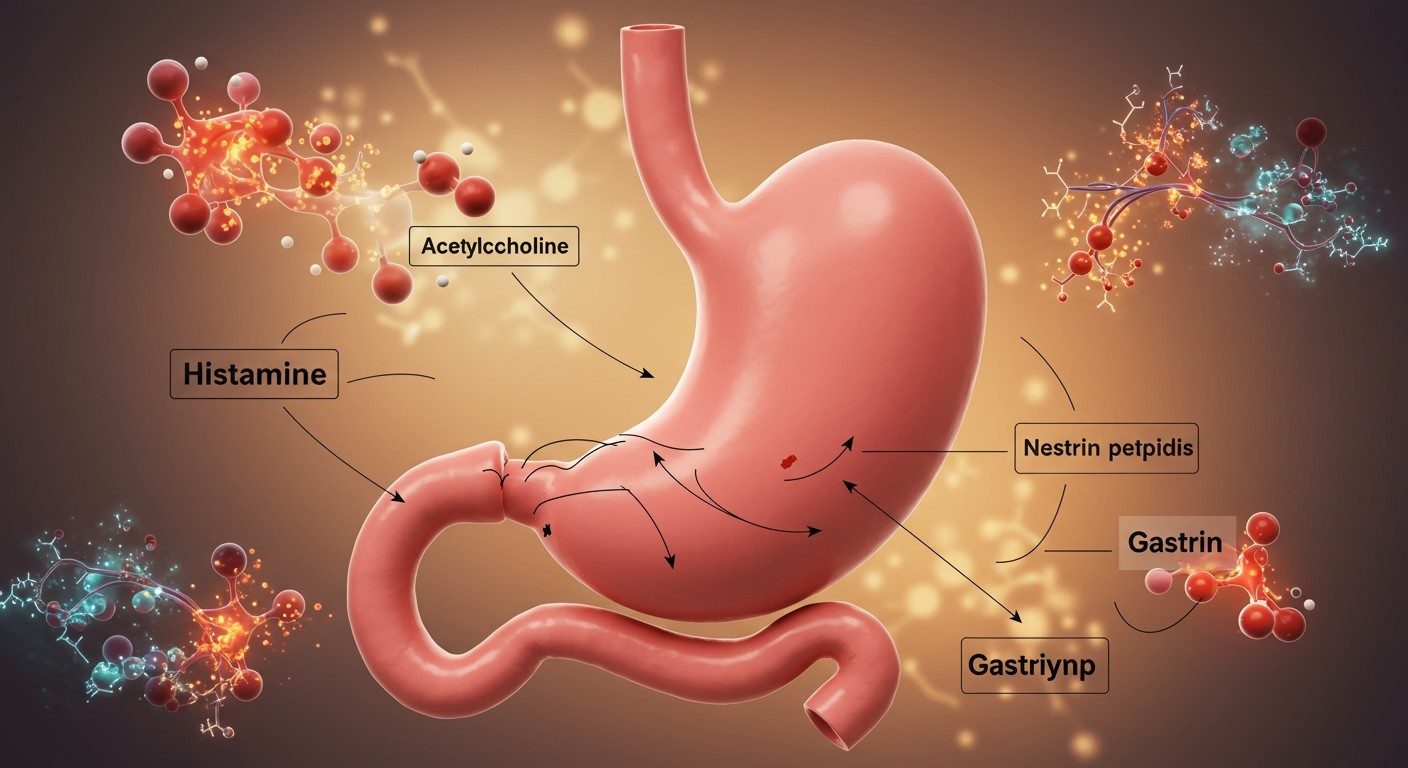
A gyomorsav szekréciójának szabályozása rendkívül összetett folyamat, melyben a protonpumpa (H+/K+ ATPáz) kulcsszerepet játszik. Ez a fehérje felelős a gyomor parietális sejtjeiben a hidrogénionok (H+) aktív transzportjáért a gyomor lumenébe, ami a gyomorsav (sósav, HCl) fő komponense. A protonpumpa működését számos tényező befolyásolja, de a legfontosabb stimuláló tényezők a hisztamin, acetilkolin és gasztrin.
Hisztamin: A ECL (enterochromaffin-like) sejtek által termelt hisztamin az egyik legerősebb gyomorsav-szekréciót serkentő anyag. A hisztamin a parietális sejteken található H2 receptorokhoz kötődik. Ez a kötődés aktiválja az adenilát-cikláz enzimet, ami növeli a sejten belüli ciklikus AMP (cAMP) szintjét. A megnövekedett cAMP aktiválja a protein kináz A-t (PKA), ami foszforilálja a protonpumpát, ezáltal növelve annak aktivitását és a gyomorsav termelését.
Acetilkolin: A bolygóideg (nervus vagus) által felszabaduló acetilkolin közvetlenül a parietális sejteken található M3 muszkarin receptorokhoz kötődik. Ez a kötődés foszfolipáz C-t aktivál, ami inozitol-trifoszfátot (IP3) és diacilglicerolt (DAG) termel. Az IP3 felszabadítja a kalciumot a sejten belüli tárolókból, míg a DAG aktiválja a protein kináz C-t (PKC). A megnövekedett kalcium-szint és a PKC aktivációja egyaránt serkenti a protonpumpa aktivitását és a gyomorsav szekrécióját.
Gasztrin: A G sejtek által a gyomor antrumában termelt gasztrin kétféleképpen serkenti a gyomorsav szekrécióját. Egyrészt, közvetlenül kötődik a parietális sejteken található CCK2 receptorokhoz, ami hasonló jelátviteli útvonalat indít el, mint az acetilkolin (foszfolipáz C aktiváció, kalcium-szint növekedése). Másrészt, a gasztrin serkenti a hisztamin felszabadulását az ECL sejtekből, így közvetetten is növeli a gyomorsav termelését.
Mindhárom stimuláló tényező (hisztamin, acetilkolin, gasztrin) végső soron a protonpumpa aktivitásának növelésével éri el a gyomorsav szekréciójának serkentését, bár eltérő jelátviteli útvonalakon keresztül.
Fontos megjegyezni, hogy ezek a stimuláló tényezők szinergikusan hatnak, ami azt jelenti, hogy együttes hatásuk nagyobb, mint az egyes tényezők hatásának összege. Például, a hisztamin, acetilkolin és gasztrin együttes jelenléte sokkal erőteljesebb gyomorsav-szekréciót eredményez, mint bármelyikük külön-külön.
A stimuláló tényezők hatása a parietális sejtekre és a protonpumpa aktivációjára
A parietális sejtek, melyek a gyomor falában találhatók, felelősek a sósav (HCl) termeléséért. A gyomorsav termelésének szabályozása egy komplex folyamat, amelyben több stimuláló tényező is szerepet játszik, közvetlenül befolyásolva a protonpumpa (H+/K+ ATPáz) aktivitását.
Három fő stimuláló tényező serkenti a parietális sejteket: acetilkolin (Ach), hisztamin és gasztrin. Mindhárom receptorokhoz kötődik a parietális sejtek membránján, elindítva egy intracelluláris jelátviteli kaszkádot.
- Acetilkolin: A vagus ideg által felszabaduló acetilkolin az M3 muszkarin receptorokhoz kötődik, ami a kalcium szintjének növekedéséhez vezet a sejtben. Ez a kalcium növekedés aktiválja a protein kináz C-t (PKC), ami közvetlenül foszforilálja és aktiválja a protonpumpát, elősegítve a savtermelést.
- Hisztamin: A hisztamin, amelyet az ECL sejtek termelnek (enterochromaffin-like cells), a H2 receptorokhoz kötődik a parietális sejteken. Ez a kötődés stimulálja az adenilát-ciklázt, ami növeli a ciklikus AMP (cAMP) szintjét. A cAMP aktiválja a protein kináz A-t (PKA), ami szintén foszforilálja és aktiválja a protonpumpát.
- Gasztrin: A gasztrin, amelyet a G sejtek termelnek, a CCK2 receptorokhoz kötődik, ami szintén a kalcium szintjének növekedéséhez vezet, hasonlóan az acetilkolinhoz.
A stimuláló tényezők együttes hatása szinergikus, azaz együttesen nagyobb mértékben növelik a savtermelést, mint külön-külön.
Fontos megjegyezni, hogy a protonpumpa aktivációja nem csupán a foszforilációtól függ. A pumpának a sejtmembránba történő beépülése is kulcsfontosságú. A stimuláló tényezők elősegítik a protonpumpa tartalmú tubulovesiculáris struktúrák (TVS) fúzióját a sejtmembránnal, növelve ezzel a működő pumpák számát a membránon. Ezzel párhuzamosan a savtermelés gátlása során a protonpumpák visszakerülnek a TVS-ekbe, csökkentve a savtermelést.
A savtermelés szabályozása tehát egy dinamikus folyamat, amelyben a stimuláló tényezők hatására a protonpumpa aktiválódik, beépül a sejtmembránba, és savat pumpál a gyomor lumenébe. Ezzel szemben a gátló tényezők a pumpa inaktivációját és internalizációját idézik elő.
A protonpumpa inhibitorok (PPI-k) hatásmechanizmusa és típusai
A protonpumpa inhibitorok (PPI-k) a gyomorsav termelést csökkentő gyógyszerek egy csoportja, amelyek közvetlenül a parietális sejtekben található H+/K+-ATPáz enzimhez, azaz a protonpumpához kötődve fejtik ki hatásukat. Ez az enzim felelős a gyomorsav (sósav, HCl) szekréciójáért a gyomor lumenébe.
A PPI-k prodrugok, ami azt jelenti, hogy inaktív formában kerülnek a szervezetbe. A véráramba felszívódva a parietális sejtekbe jutnak, ahol a savas környezet aktiválja őket. Az aktiváció során a PPI molekulák átalakulnak egy aktív szulfénamid származékká. Ez a származék kovalens kötést alakít ki a protonpumpa cisztein aminosavmaradványaival, irreverzibilisen gátolva annak működését.
Mivel a PPI-k irreverzibilisen gátolják a protonpumpát, a gyomorsav termelés csak akkor tér vissza a normális szintre, amikor új protonpumpák szintetizálódnak. Ez a folyamat körülbelül 18-24 órát vesz igénybe, ezért a PPI-k hatása elhúzódó, és napi egyszeri adagolás is elegendő lehet.
A legfontosabb tudnivaló, hogy a PPI-k a működő protonpumpákat gátolják, ezért a legjobb hatás elérése érdekében a gyógyszert étkezés előtt kell bevenni, amikor a protonpumpák aktív állapotban vannak.
Számos különböző PPI áll rendelkezésre, amelyek kémiai szerkezetükben és metabolizmusukban különböznek egymástól. Néhány gyakran használt PPI közé tartozik:
- Omeprazol
- Lansoprazol
- Pantoprazol
- Rabeprazol
- Esomeprazol (az omeprazol S-izomerje)
Bár a PPI-k hasonló hatásmechanizmussal rendelkeznek, kisebb különbségek lehetnek a hatékonyságukban, a mellékhatásaikban és a gyógyszerkölcsönhatásaikban. Az orvos a beteg állapotának és egyéb gyógyszereinek figyelembevételével választja ki a legmegfelelőbb PPI-t.
A PPI-k széles körben alkalmazottak a gyomorsavval kapcsolatos problémák kezelésére, mint például a gyomorfekély, a nyombélfekély, a refluxbetegség (GERD) és a Zollinger-Ellison szindróma. Fontos azonban, hogy a PPI-ket orvosi felügyelet mellett szedjük, mivel hosszan tartó használatuk mellékhatásokkal járhat.
A PPI-k metabolizmusa és farmakokinetikája
A protonpumpa-gátlók (PPI-k) hatékonysága a gyomorsav-szekréció szabályozásában nagyrészt metabolizmusuk és farmakokinetikájuk függvénye. A PPI-k gyenge bázisok, melyek a gyomor parietális sejtjeinek savas környezetébe jutva protonálódnak és aktív formájukká alakulnak. Ez az aktiváció irreverzibilisen gátolja a H+/K+-ATPáz enzimet, azaz a protonpumpát.
A PPI-k felszívódása a vékonybélből történik, de a gyomorsav instabillá teszi őket, ezért enteroszolvens bevonattal rendelkeznek. A felszívódás után a PPI-k a májba jutnak, ahol nagyrészt a CYP2C19 és a CYP3A4 enzimek metabolizálják őket. Az egyének közötti genetikai variációk a CYP2C19 enzim aktivitásában jelentős különbségeket eredményezhetnek. Ez befolyásolja a PPI-k plazmakoncentrációját és ezáltal a terápiás hatékonyságot. Például a „gyors metabolizálók” esetében a PPI-k gyorsabban lebomlanak, ami alacsonyabb plazmaszintekhez és esetlegesen csökkent hatékonysághoz vezethet.
A PPI-k rövid felezési ideje (általában 1-2 óra) ellenére tartósan csökkentik a gyomorsav-szekréciót, mivel a protonpumpát irreverzibilisen gátolják. Új protonpumpák szintézise szükséges a gyomorsav-szekréció helyreállításához.
A PPI-k adagolásának időzítése is fontos tényező. A legjobb, ha étkezés előtt 30-60 perccel veszik be őket, amikor a protonpumpák a legaktívabbak. Ez maximalizálja a gyógyszer hatását a savtermelésre.
A PPI-k klinikai alkalmazása: gyomorfekély, refluxbetegség, Zollinger-Ellison szindróma
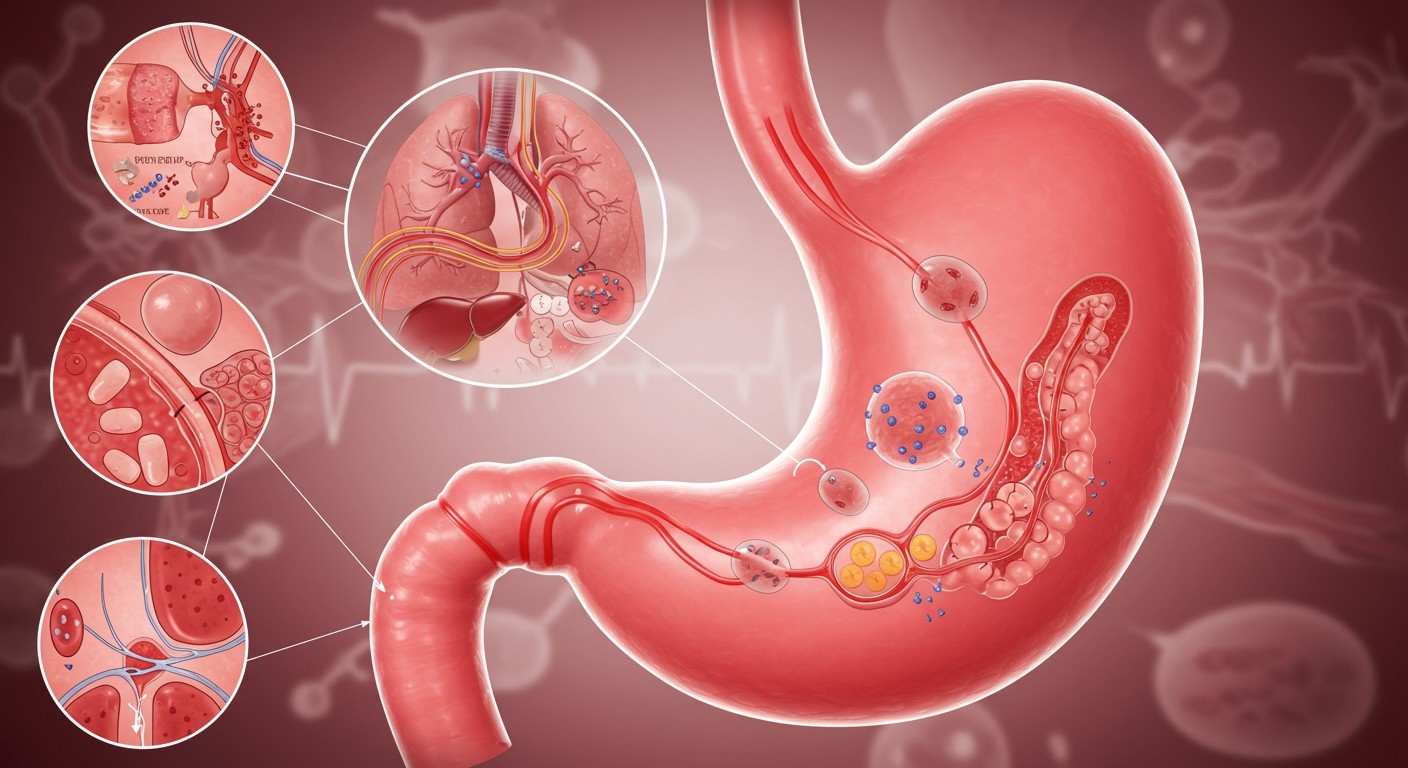
A protonpumpa-gátlók (PPI-k) a gyomorsavszekréció csökkentésének leghatékonyabb eszközei, és széles körben alkalmazzák őket a gyomor-bélrendszeri betegségek kezelésében. Hatásuk azon alapul, hogy irreverzibilisen blokkolják a H+/K+-ATPáz enzimet, más néven a protonpumpát, amely a gyomor parietális sejtjeinek membránjában található és a gyomorsav termeléséért felelős.
A gyomorfekély esetén a PPI-k kulcsfontosságúak a gyógyulás elősegítésében és a fájdalom csökkentésében. A savszekréció gátlásával a PPI-k lehetővé teszik a fekélyes terület hámosodását és a gyulladás csökkenését. Gyakran kombinálják őket antibiotikumokkal a Helicobacter pylori eradikálására, ami a fekélyek egyik legfőbb okozója.
A refluxbetegség (GERD) a gyomortartalom nyelőcsőbe való visszajutásával jár, ami gyomorégést, savas felböfögést és egyéb kellemetlen tüneteket okoz. A PPI-k hatékonyan csökkentik a gyomorsav mennyiségét, ezáltal enyhítve a tüneteket és lehetővé téve a nyelőcső nyálkahártyájának gyógyulását. A PPI-k gyakran hosszú távú kezelést jelentenek a súlyosabb esetekben, bár a mellékhatások elkerülése érdekében a legkisebb hatékony dózist kell alkalmazni.
A Zollinger-Ellison szindróma egy ritka betegség, amelyet gastrin-termelő daganat okoz, ami túlzott gyomorsavtermeléshez vezet. A PPI-k ebben az esetben életmentőek lehetnek, mivel a magas dózisú PPI-kezelés képes kontrollálni a savszintet és megelőzni a súlyos szövődményeket, mint például a fekélyeket, vérzést és a nyelőcső károsodását.
Fontos megjegyezni, hogy a PPI-k használata nem kockázatmentes. Hosszú távú használatuk összefüggésbe hozható bizonyos mellékhatásokkal, mint például a Clostridium difficile fertőzés kockázatának növekedése, a csontritkulás és a B12-vitamin hiány. Ezért a PPI-k alkalmazását mindig orvosi felügyelet mellett kell végezni, és a kezelés időtartamát a lehető legrövidebbre kell korlátozni.
A PPI-k mellékhatásai és a hosszú távú használat kockázatai
Bár a protonpumpa-gátlók (PPI-k) hatékonyan csökkentik a gyomorsav termelését, hosszú távú használatuk számos mellékhatással és kockázattal járhat. Ezek a gyógyszerek, miközben enyhítik a savas reflux tüneteit, befolyásolhatják a tápanyagok felszívódását és a szervezet természetes védekező mechanizmusait.
Az egyik leggyakoribb probléma a B12-vitamin felszívódásának csökkenése. A gyomorsav szükséges a B12-vitamin fehérjékhez kötött formájának felszabadításához, így a PPI-k használata hiányt okozhat, ami idegrendszeri problémákhoz és vérszegénységhez vezethet. Hasonlóan, a magnézium felszívódása is romolhat, ami izomgörcsöket, szívritmuszavarokat és fáradtságot eredményezhet.
A gyomorsav fontos szerepet játszik a kórokozók elpusztításában is. A PPI-k által okozott savszint csökkenés növelheti a fertőzések kockázatát, például a Clostridium difficile okozta hasmenés (CDI) vagy a tüdőgyulladás kialakulásának esélyét.
A legfontosabb kockázat talán az, hogy a hosszú távú PPI-használat összefüggésbe hozható a csontritkulással és a csípőtáji törések megnövekedett kockázatával, különösen idősebb betegeknél.
Ezen felül, egyes kutatások összefüggést találtak a PPI-k és a krónikus vesebetegség, valamint a demencia kialakulása között, bár ezek az eredmények még további vizsgálatokat igényelnek. A PPI-k hirtelen elhagyása „rebound” hatást okozhat, ami a gyomorsav túlzott termeléséhez vezet, és a tünetek visszatéréséhez.
Fontos, hogy a PPI-ket csak orvosi javaslatra és a lehető legrövidebb ideig használjuk. Amennyiben lehetséges, érdemes alternatív kezelési módokat keresni, például életmódbeli változtatásokat és más gyógyszereket, amelyek kevésbé befolyásolják a gyomorsav termelését.
A gyomorsav szekréciójának egyéb szabályozó mechanizmusai: szomatosztatin, prostaglandinok
A protonpumpa működését nem csak a hisztamin, acetilkolin és gasztrin szabályozza. Fontos szerep jut a szomatosztatin és a prostaglandinoknak is a gyomorsav szekréciójának finomhangolásában. A szomatosztatin, egy peptid hormon, gátló hatást fejt ki a gyomor parietális sejtjeire. Ez azt jelenti, hogy csökkenti a protonpumpa aktivitását és ezáltal a sósav termelését. A szomatosztatin termelése a gyomorban válaszként nőhet a gyomorsav túlzott szekréciójára, ezáltal egy negatív visszacsatolási mechanizmust alkotva.
A prostaglandinok, mint az PGE2 és PGI2, szintén védelmező szerepet töltenek be a gyomorban. Stimulálják a nyálkahártya és a bikarbonát termelését, amelyek védik a gyomor falát a sav káros hatásaitól. Ezen kívül, a prostaglandinok közvetlenül gátolják a parietális sejtek által történő sav szekréciót, csökkentve a protonpumpa működését.
A nem-szteroid gyulladáscsökkentő gyógyszerek (NSAID-ok) gátolják a prostaglandinok szintézisét, ami növelheti a gyomorsav szekréciót és a gyomorfekély kockázatát.
Tehát, a szomatosztatin és a prostaglandinok kulcsfontosságú szerepet játszanak a gyomorsav szekréciójának negatív szabályozásában, hozzájárulva a gyomor pH-jának homeosztázisához és a gyomor nyálkahártyájának védelméhez.
A Helicobacter pylori szerepe a gyomorsav termelésben és a protonpumpa szabályozásában
A Helicobacter pylori (H. pylori) baktérium kulcsszerepet játszik a gyomorsav termelés szabályozásában, és ezáltal a protonpumpák (H+/K+ ATPáz) működésének befolyásolásában is. Bár elsőre paradoxnak tűnhet, a H. pylori hatása összetett, és a fertőzés helyétől, a baktérium törzsétől, valamint a gazdaszervezet genetikai adottságaitól függ.
A H. pylori elsősorban a gyomor antrumát (alsó részét) kolonizálja. Itt az általa termelt ureáz enzim ammóniát (NH3) állít elő a karbamidból (urea). Az ammónia semlegesíti a gyomorsavat a baktérium környezetében, lehetővé téve annak túlélését. Az ammónia azonban egyben serkenti a G-sejtek fokozott gasztrin termelését. A gasztrin, egy hormon, a véráramba kerülve eléri a gyomor fundusában (felső részében) található parietális sejteket, és stimulálja a protonpumpákat, amelyek a gyomorsavat termelik.
A krónikus H. pylori fertőzés azonban a gyomor nyálkahártyájának gyulladásához vezet (gasztritisz). A gyulladás citokineket szabadít fel, amelyek gátolhatják a parietális sejtek működését, ezáltal csökkentve a gyomorsav termelést. Egyes H. pylori törzsek, különösen a CagA-pozitív törzsek, erősebb gyulladást okoznak, és nagyobb valószínűséggel vezetnek a gyomorsav termelés csökkenéséhez, ami növeli a gyomorrák kockázatát.
A H. pylori fertőzés tehát nem egyértelműen a gyomorsav termelés növekedéséhez vezet, hanem egy dinamikus folyamat, amely a gyulladás mértékétől és a baktérium virulencia faktoraitól függően változhat.
A protonpumpa gátló (PPI) gyógyszerek alkalmazása H. pylori fertőzés esetén különös figyelmet igényel. Mivel a PPI-k csökkentik a gyomorsav szintjét, a baktériumok a gyomor felsőbb részeibe vándorolhatnak, ami növelheti a testállomány gyulladásának és a gyomorrák kockázatának a veszélyét. Ezért a H. pylori fertőzött betegeknél, akik PPI-t szednek, fontos a baktérium eradikálása (kiirtása).
A diéta és életmód hatása a gyomorsav szintre és a protonpumpa működésére

A diéta és az életmód jelentős befolyással bír a gyomorsav szintre, és ezen keresztül a protonpumpák működésére. Bizonyos ételek és italok serkenthetik a gyomorsav termelését, míg mások éppen ellenkezőleg, csökkenthetik azt. Például, a zsíros, fűszeres ételek, a koffein, az alkohol és a szénsavas italok fokozhatják a gyomorsav szekrécióját, ami a protonpumpák fokozott aktivitásához vezethet.
Másrészt, a rostban gazdag étrend, a sovány fehérjék és a lúgosító hatású zöldségek segíthetnek a gyomorsav szintjének szabályozásában, ezáltal csökkentve a protonpumpák terhelését.
Az életmódbeli tényezők, mint a stressz és a dohányzás is befolyásolják a gyomorsav termelését. A stressz fokozhatja a gyomorsav szekrécióját, míg a dohányzás gyengítheti a nyelőcső záróizmát, ami savas refluxhoz vezethet. A rendszeres testmozgás és a megfelelő alvás segíthet a stressz kezelésében és a gyomor-bélrendszer egészségének megőrzésében.
A tudatos táplálkozás, mely magában foglalja a gyomorsav termelést fokozó ételek kerülése mellett a rendszeres, kisebb étkezéseket, kulcsfontosságú a gyomorsav szintjének optimális szabályozásában és a protonpumpák egészséges működésének fenntartásában.
Fontos megjegyezni, hogy mindenki szervezete másképp reagál az egyes ételekre és életmódbeli tényezőkre. Ezért érdemes odafigyelni a saját testünk jelzéseire, és szükség esetén szakember segítségét kérni a megfelelő diéta és életmód kialakításához.